TCR サービスの内容
- TCR スクリーニングの実施において 20 年以上の経験とノウハウを持つサイエンティストの専任チーム
- 新しい抗体クラス(マウス、ヒト化、キメラ、完全ヒト、抗体カクテル、Fab/VH フラグメント、融合タンパク質、二重特異性スーパー抗原、ビオマー、四量体、ナノボディなど)や、キャリアバックボーンに属するさまざまな地域のプロトコル開発に関する経験と専門知識
- カスタム抗体 / タンパク質の標識化サービス
- 経験豊富な専任のサイエンティストによる IHC 染色プロトコルの開発と最適化 - 有意義で確かな交差反応性データを生成
- 組織学および IHC に関する広範な知識を持つ経験豊かな試験責任者によるアドバイスと指導 認可を受けた施設 - FDA と EMA の規制ガイドラインを満たす質の高いヒトや動物の凍結組織を使用
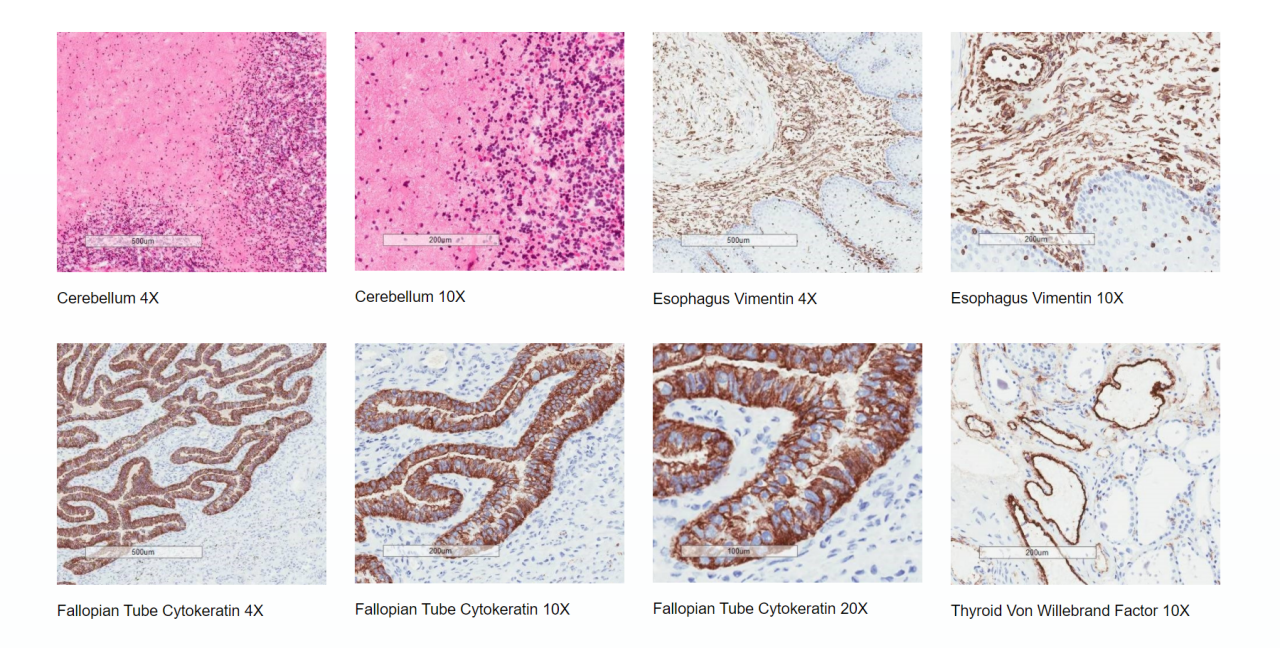
- 各試験に対する組織の適合性評価 - 組織と抗原の完全性を維持(下記画像を参照)
- 手動および自動の IHC 染色プラットフォーム - 柔軟性と IHC 法のカスタマイズを実現
- TCR 評価における染色の評価と解釈に関する経験を持つ専門分野の病理学者(MRCPath、FRCPath、米国の認定資格あり)
- 試験のエンドポイント達成をサポートする柔軟なレポーティング基準